विद्युत संयोजी या आयनिक आबंध, लक्षण, गुण और उदाहरण लिखिए, बंध
विद्युत संयोजी आबंध
दो असमान परमाणुओं के मध्य इलेक्ट्रॉनों के स्थानांतरण से जो बंध श बनते हैं। उन्हें विद्युत संयोजी या आयनिक बंध (electrovalent or ionic bond) कहते हैं। तथा इस प्रकार बने यौगिकों को विद्युत संयोजी यौगिक कहते हैं।
अर्थात् दो परमाणुओं में से एक परमाणु इलेक्ट्रॉन त्यागकर तथा दूसरों परमाणु इलेक्ट्रॉन ग्रहण करके अक्रिय गैस की स्थायी संरचना प्राप्त कर लेते हैं। इस प्रकार बने आबंध को विद्युत संयोजी आबंध कहते हैं।
विद्युत संयोजी या आयनिक बंध के उदाहरण
1. सोडियम क्लोराइड (NaCl) का बनना –
सोडियम परमाणु के बाह्य कोश में एक इलेक्ट्रॉन होता है। तथा कैल्शियम परमाणु के बाह्य कोश में सात इलेक्ट्रॉन होते हैं।
अतः सोडियम एक इलेक्ट्रॉन को कैल्शियम परमाणु को देकर अक्रिय गैस की स्थायी संरचना प्राप्त कर लेता है। और कैल्शियम एक इलेक्ट्रॉन को लेकर अक्रिय गैस की स्थायी संरचना प्राप्त कर लेता है। तथा Na और Cl दोनों Na+ तथा Cl– आयन में बदल जाते हैं।
Na = 11 = 2, 8, 1
Cl = 17 = 2, 8, 7
Na = 11 = 2, 8, 1
Cl = 17 = 2, 8, 7
x = Na परमाणु के इलेक्ट्रॉन
• = Cl परमाणु के इलेक्ट्रॉन
इसमें Na की विद्युत संयोजकता +1 तथा Cl की विद्युत संयोजकता -1 है।
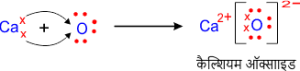
2. कैलशियम ऑक्साइड (CaO) का बनना –
Ca = 20 = 2, 8, 8, 2
O = 8 = 2, 6
इसमें Ca की विद्युत संयोजकता +2 तथा O की विद्युत संयोजकता -2 है।
3. मैग्नीशियम क्लोराइड (MgCl2) का बनना –
Mg = 12 = 2, 8, 2
Cl = 17 = 2, 8, 7
Cl = 17 = 2, 8, 7
Note – जब एक परमाणु से दूसरे परमाणु में इलेक्ट्रॉनों का स्थानांतरण होता है। तो परमाणु विपरीत आवेशित आयनों में बदल जाते हैं। यह स्थिर विद्युत बलों द्वारा जुड़े रहते हैं। विपरीत आवेशित आयनों को बांधे रखने वाले बंध को आयनिक बंध कहते हैं।
विद्युत संयोजी यौगिक धनावेशित और ऋणावेशित आयनों से बंधे होते हैं। अर्थात् विद्युत संयोजी यौगिक अणुओं से नहीं सीधे आयनों से बने होते हैं। जिस कारण इनकी प्रकृति आयनित होती है।
विद्युत संयोजी यौगिक के लक्षण
1. विद्युत संयोजी या आयनिक यौगिक विद्युत आवेशित परमाणु द्वारा बने होते हैं।
2. विद्युत संयोजी या आयनिक यौगिकों के मध्य प्रबल आकर्षक बल होता है जिस कारण इनके गलनांक और क्वथनांक उच्च होते हैं।
3. यह यौगिक जल तथा ध्रुवीय विलायकों में विलेय होते हैं। लेकिन यह अध्रुवीय विलायकों में अविलेय होते हैं।
4. गलित अवस्था में यह विद्युत के सुचालक होते हैं।
विद्युत संयोजी आबंध और सहसंयोजक आंबध में अंतर
| क्रम संख्या | विद्युत संयोजी आबंध | सहसंयोजक आबंध |
| 1 | यह आबंध इलेक्ट्रॉनों के स्थानांतरण द्वारा बनते हैं। | यह आबंध परस्पर साझे के इलेक्ट्रॉन युग्म द्वारा बनते हैं। |
| 2 | यह सदैव असमान परमाणुओं के मध्य ही बनते हैं। | यह समान और असमान दोनों प्रकार परमाणुओं के मध्य ही बनते हैं। |
| 3 | विद्युत संयोजी यौगिक जल में विलेय होते हैं। | सहसंयोजक यौगिक जल में अविलेय होते हैं। |
| 4 | यह आबंध ध्रुवीय होते हैं। तथा यह धनावेशित एवं ऋणावेशित ध्रुव होते हैं। | यह आबंध ध्रुवीय तथा अध्रुवीय दोनों प्रकार के होते हैं। |


Leave a Reply