d एवं f ब्लॉक के तत्व
प्रश्न 1. निम्नलिखित की व्याख्या करें:
(i) \(Sc^{3+}, Co^{2+}\) और \(Cr^{3+}\) आयनों में से, केवल \(Sc^{3+}\) जल में रंगहीन है। (परमाणु संख्या: Co = 27; Sc = 21 और Cr = 24)
(ii) ताम्र धातु के लिए E°\(Cu^2\) + / Cu का मान धनात्मक (+0.34) है, जबकि पहली संक्रमण श्रेणी के शेष सदस्यों के लिए यह ऐसा नहीं है।
(iii) \(La(OH)_3, Lu(OH)_3\) की तुलना में अधिक क्षारीय है।
उत्तर:
(i) \(Co^{2+}: \) [Ar] \(3d^{7},Sc^{3+}: \) [Ar]\(3d° Cr^{3+}: \)[Ar] \(3d^{3} Co^{2+} और Cr^{3+}\) में अप्रतिबंधित इलेक्ट्रॉन होते हैं, इसलिए वे जलीय घोल में रंगीन होते हैं।
\(Sc^{3+}\) में कोई अप्रतिबंधित इलेक्ट्रॉन नहीं होता, इसलिए यह रंगहीन होता है।
(ii) धातु ताम्र की परमाणुकरण एंथैल्पी और आयनीकरण एंथैल्पी उच्च होती है। इसलिए, Cu(s) को \(Cu^{2+}(aq)\) में बदलने के लिए आवश्यक उच्च ऊर्जा उसकी जलयोजन एंथैल्पी द्वारा संतुलित नहीं होती।
(iii) लैन्थेनाइड संकुचन के कारण, लैन्थेनाइड आयन का आकार परमाणु संख्या बढ़ने के साथ नियमित रूप से घटता जाता है। इस कारण \(La(OH)_3 \)से \(Lu(OH)_3\) की हाइड्रॉक्साइड्स की क्षारीयता कम होती जाती है।
प्रश्न 2. (a) निम्नलिखित रासायनिक अभिक्रियाओं को पूरा करें:
(i) \(2MnO_4 ^-\) \( + 5 NO_2 ^- + 6 H^+ →\)
(ii) \(3MnO_4 ^- + 4 H^+ →\)
(b) लैंथेनाइड श्रृंखला के एक सदस्य का नाम बताएं जो +4 ऑक्सीकरण अवस्था प्रदर्शित करता है।
उत्तर: सेरियम / Ce
प्रश्न 3. निम्नलिखित के लिए कारण बताएं:
(i) \(Min^{3+}/Min^{2+}\) युग्म के लिए E° मान \(Fe^{3+}/Fe^{2+}\) की तुलना में बहुत अधिक धनात्मक होता है।
(ii) तांबे (Cu) की तुलना में लौह (Fe) का परमाणुकरण एन्थैल्पी अधिक होती है।
(iii) \(Sc^{3+}\) जल में रंगहीन है जबकि \(Ti^{3+}\) रंगीन है।
उत्तर:
(i) Mn का उच्च मान यह दर्शाता है कि Mn विशेष रूप से स्थिर है। Mn के तीसरे आयनीकरण ऊर्जा में बदलाव \((d^6)\) से \((d^5)\) से में होता है, जो स्थिरता प्रदान करता है।
(ii) लौह (Fe) में अपवित्र इलेक्ट्रॉनों की अधिक संख्या के कारण इसका परमाणुकरण एन्थैल्पी तांबे (Cu) से अधिक होती है।
(iii) \(Sc^{3+}\) में अपवित्र d-इलेक्ट्रॉन की अनुपस्थिति होती है, जबकि \(Ti^{3+}\) में एक अपवित्र इलेक्ट्रॉन होता है, जो d-d संक्रमण को प्रदर्शित करता है और इसलिए यह रंगीन होता है।
प्रश्न 4: निम्नलिखित रासायनिक समीकरणों को पूरा करें:
(a) \(MnO_4^-(aq) + SO_3^{2-}(aq) + H_2O(l) →\)
(b) \(Cr_2O_7^{2-}(aq) + Fe^{2+}(aq) + H^+(aq) →\)
उत्तर:
(ii) निम्नलिखित अवलोकनों के लिए एक स्पष्टीकरण दें:
(a) \(La^{3+} (Z = 57)\) और \(Lu^{3+} (Z = 71)\) घोलों में कोई रंग नहीं दिखाते हैं।
उत्तर:
\(La^{3+}\) में कोई f-इलेक्ट्रॉन नहीं होता और \(Lu^{3+}\) में 4f उप-खण्ड पूरा होता है (\(4f^{14}\)) इसलिए, यहाँ कोई अपैरड इलेक्ट्रॉन नहीं होता और परिणामस्वरूप d-d ट्रांजिशन संभव नहीं होते। इसलिए, \(La^{3+}\) और \(Lu^{3+}\) घोलों में कोई रंग नहीं दिखाते हैं।
(b) पहले संक्रमण श्रृंखला में द्विसंयोजी आयनों में मैंगनीज सबसे अधिक पैरा-मैग्नेटिकता प्रदर्शित करता है।
उत्तर:
पहले संक्रमण श्रृंखला में द्विसंयोजी आयनों में मैंगनीज (Z = 25) सबसे अधिक पैरा-मैग्नेटिकता प्रदर्शित करता है क्योंकि इसमें सबसे अधिक अपैरड इलेक्ट्रॉन (\(3d^5\) होते हैं।
(c) \(Cu^{1+}\) आयन जल में ज्ञात नहीं होता।
उत्तर:
जल में \(Cu^{1+}\) का अनुपातिकरण हो जाता है और यह \(Cu^{2+}\) और धातु में बदल जाता है।
\(2Cu^{1+} → Cu^{2+} + Cu\)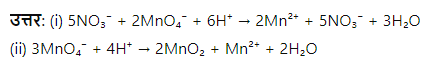
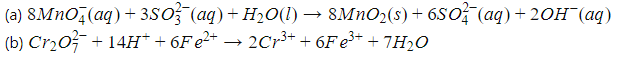
Leave a Reply